با بازطراحی یک داروی شیمیدرمانی رایج، دانشمندان قدرت اثرگذاری آن را ۲۰ هزار برابر افزایش دادند. در یک گام مهم برای درمان سرطان، پژوهشگران دانشگاه نورثوسترن ساختار مولکولی یک داروی شناختهشده شیمیدرمانی را بازطراحی کردهاند و بدین ترتیب حلالیت، اثربخشی و ایمنی آن بهطور چشمگیری افزایش یافته است.
در این مطالعه، دانشمندان دارو را کاملاً از ابتدا به شکل «اسید نوکلئیک کروی» (SNA) تولید کردند؛ ساختاری در مقیاس نانو که دارو را در رشتههای DNA احاطهکنندهی کرههای کوچک جایگذاری میکند. این طراحی نوآورانه، ترکیبی که معمولاً حلالیت کمی دارد و اثر آن ضعیف است را به درمانی بسیار قدرتمند و هدفمند تبدیل میکند که به سلولهای سالم آسیبی نمیرساند.
وقتی نسخهی مبتنی بر SNA در مدل حیوانی مبتلا به «لوسمی میلوئید حاد» (AML)، نوعی سرطان خون تهاجمی و دشوار برای درمان، آزمایش شد، نتایج قابل توجهی نشان داد. این دارو ۱۲.۵ برابر بهتر وارد سلولهای لوسمی شد، تا ۲۰ هزار برابر مؤثرتر آنها را از بین برد و سرعت پیشرفت سرطان را ۵۹ برابر کاهش داد، بدون اینکه عوارض جانبی قابل توجهی ایجاد کند.
به گفتهی پژوهشگران، این دستاورد نشاندهندهی پتانسیل روزافزون «نانوپزشکی ساختاری» است؛ حوزهای نوظهور که در آن دانشمندان ساختار و ترکیب داروهای نانو را با دقت طراحی میکنند تا رفتار آنها در بدن کنترل شود. با هفت درمان مبتنی بر SNA که هماکنون در آزمایشهای بالینی قرار دارند، این رویکرد میتواند مسیر ساخت واکسنهای پیشرفته و درمانهای نوین برای سرطان، بیماریهای عفونی، اختلالات عصبی و بیماریهای خودایمنی را هموار کند.
پیشرفت بزرگی با وعده بالینی
چاد اِی. میرجین از دانشگاه نورثوسترن که رهبری این مطالعه را بر عهده داشت، گفت: «در مدلهای حیوانی نشان دادیم که میتوانیم رشد تومورها را متوقف کنیم. اگر این نتایج در بیماران انسانی نیز تکرار شود، یک پیشرفت بسیار هیجانانگیز خواهد بود. این به معنای شیمیدرمانی مؤثرتر، نرخ پاسخدهی بهتر و عوارض جانبی کمتر است. این همیشه هدف هر نوع درمان سرطان است.»
میرجین که از پیشگامان شیمی و نانوپزشکی محسوب میشود، استاد علوم شیمی، مهندسی شیمی و زیستی، مهندسی پزشکی، علم و مهندسی مواد و پزشکی در دانشگاه نورثوسترن است و در کالج هنر و علوم وینبرگ، دانشکده مهندسی مککورمیک و دانشکده پزشکی فاینبرگ نیز فعالیت دارد. او همچنین بنیانگذار موسسه بینالمللی نانوتکنولوژی و عضو مرکز جامع سرطان رابرت اچ. لوری دانشگاه نورثوسترن است.
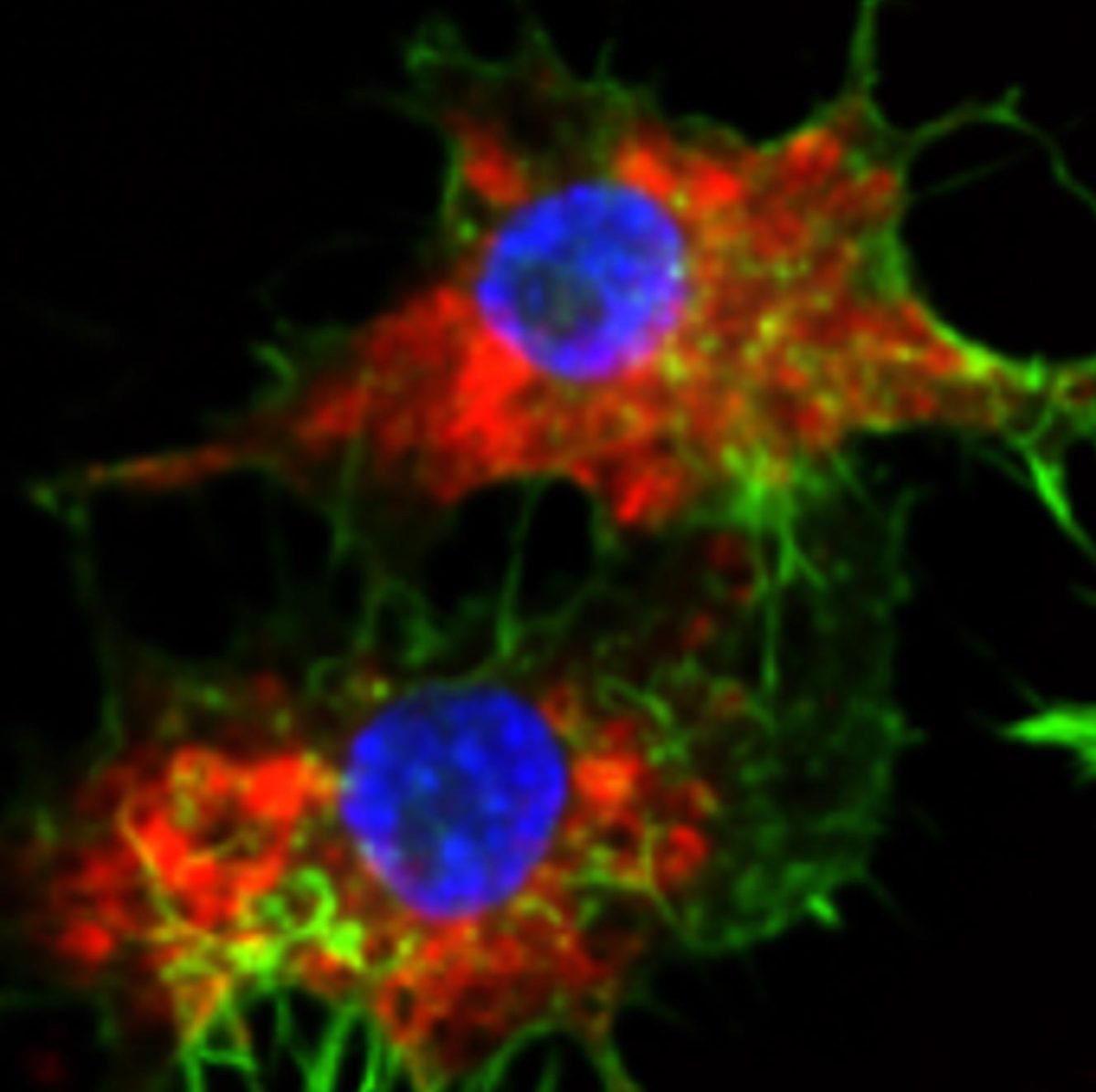
تصویر میکروسکوپی نشاندهنده جذب SNAها در سلولهای لوسمی
SNAها به رنگ قرمز و هستههای سلولی به رنگ آبی نمایش داده شدهاند.
برای این مطالعه جدید، میرجین و تیم او بر داروی شیمیدرمانی سنتی ۵-فلورواوراسیل (5-Fu) تمرکز کردند، دارویی که اغلب نمیتواند بهطور مؤثر به سلولهای سرطانی برسد. علاوه بر این، چون این دارو به بافت سالم هم آسیب میرساند، باعث بروز عوارض جانبی متعددی از جمله تهوع، خستگی و در موارد نادر حتی نارسایی قلبی میشود.
به گفته میرجین، مشکل از خود دارو نیست، بلکه نحوه پردازش آن توسط بدن است. ۵-Fu حلالیت کمی دارد، به این معنا که کمتر از ۱٪ آن در بسیاری از مایعات بیولوژیکی حل میشود. اکثر داروها باید در جریان خون حل شوند تا بتوانند در سراسر بدن حرکت کرده و وارد سلولها شوند. اگر دارویی حلالیت پایینی داشته باشد، به صورت توده یا جامد باقی میماند و بدن نمیتواند آن را بهطور مؤثر جذب کند.
میرجین گفت: «همه ما میدانیم که شیمیدرمانی اغلب بسیار سمی است، اما بسیاری از مردم نمیدانند که اغلب حلالیت پایینی هم دارد، بنابراین ما باید راههایی پیدا کنیم تا آن را به شکل قابل حل در آب تبدیل کرده و بهطور مؤثر تحویل دهیم.»
راهکار SNA
برای توسعه یک سیستم انتقال مؤثرتر، میرجین و تیمش به سمت SNAها روی آوردند. این ساختارهای کروی نانویی که توسط میرجین در دانشگاه نورثوسترن اختراع و توسعه یافتهاند، شامل یک هسته نانوذرهای هستند که توسط یک پوشش متراکم از DNA یا RNA احاطه شده است. در مطالعات قبلی، میرجین دریافت که سلولها SNAها را شناسایی کرده و آنها را به داخل خود میپذیرند. در مطالعه جدید، تیم او SNAهای جدیدی ساخت که داروی شیمیدرمانی مستقیماً در رشتههای DNA آنها وارد شده بود.
میرجین گفت: «اکثر سلولها گیرندههای پاککننده (scavenger) روی سطح خود دارند، اما سلولهای میلوئیدی این گیرندهها را بیش از حد بیان میکنند، بنابراین تعداد آنها بسیار بیشتر است. اگر یک مولکول را شناسایی کنند، آن را به داخل سلول میکشند. به جای اینکه دارو مجبور باشد وارد سلول شود، SNAها بهطور طبیعی توسط این گیرندهها جذب میشوند.»
همانطور که میرجین و تیمش پیشبینی کرده بودند، بازطراحی ساختاری رفتار ۵-Fu را با سلولهای سرطانی کاملاً تغییر داد. برخلاف مولکولهای شیمیدرمانی آزاد و بدون ساختار، سلولهای میلوئیدی بهراحتی SNAها را شناسایی و جذب کردند. پس از ورود به سلول، آنزیمها پوشش DNA را تجزیه کرده و مولکولهای دارو را آزاد کردند که سلول سرطانی را از درون از بین بردند.
در آزمایشهای موش، این درمان سلولهای لوسمی را تقریباً بهطور کامل در خون و طحال از بین برد و طول عمر حیوانات را بهطور قابل توجهی افزایش داد. و چون SNAها بهطور انتخابی سلولهای AML را هدف قرار میدادند، بافتهای سالم آسیبی ندیدند.
میرجین افزود: «شیمیدرمانیهای امروزی هر چیزی را که ملاقات کنند از بین میبرند، بنابراین سلولهای سرطانی و بسیاری از سلولهای سالم هم نابود میشوند. نانوپزشکی ساختاری ما ترجیحاً سلولهای میلوئیدی را هدف میگیرد. به جای اینکه بدن را با شیمیدرمانی غرق کنیم، دوز بالاتر و متمرکزتری را دقیقاً به جایی میرساند که نیاز است.»
تیم میرجین در گام بعدی قصد دارد این استراتژی جدید را روی گروه بزرگتری از مدلهای حیوانی کوچک آزمایش کند، سپس به مدل حیوانی بزرگتر و در نهایت در آزمایشهای بالینی انسانی، پس از تأمین بودجه، منتقل شود.
منبع خبر : scitechdaily.com






نظرات کاربران